 Хорошо известно, что бумажный лист к пальцам не прилипает. Но стоит смочить пальцы водой, как ситуация меняется. (Этот «принцип», кстати, лежит в основе не очень хорошей привычки мусолить пальцы при чтении.) Почему же капелька воды вызывает такое разительное изменение? Хорошо известно, что бумажный лист к пальцам не прилипает. Но стоит смочить пальцы водой, как ситуация меняется. (Этот «принцип», кстати, лежит в основе не очень хорошей привычки мусолить пальцы при чтении.) Почему же капелька воды вызывает такое разительное изменение?
Чтобы разобраться в этом вопросе, нам придется обратиться к молекулярному устройству жидкости. В глубине воды, налитой, предположим, в стакан, каждая молекула окружена совершенно равномерно другими такими же молекулами воды. Поэтому во всех направлениях эта молекула испытывает одинаковые силы притяжения. Совсем иное положение у молекулы воды, находящейся на поверхности: снизу ее притягивают такие же, как и она, молекулы жидкости, а вот сверху над ней лишь изредка проносятся молекулы газов, входящих в состав воздуха. Равнодействующая сил притяжения, действующих на такую молекулу, стремится втянуть ее с поверхности в объем жидкости.
По этой причине увеличение поверхности жидкости требует некоторой затраты энергии. Возьмите стакан с водою и наклоните его. Площадь поверхности воды увеличится. Если разделить затраченную для этого энергию на приращение поверхности, мы получим весьма важную характеристику, называемую коэффициентом поверхностного натяжения.
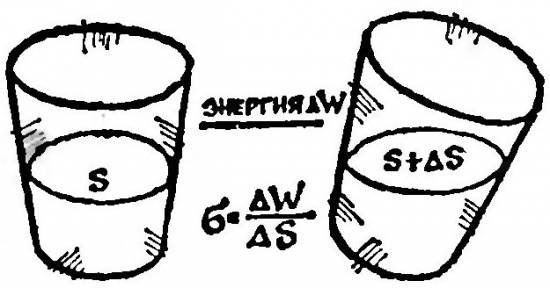
Посмотрим на дело с другой стороны. Увеличив поверхность, вы повысили энергию системы. Но самопроизвольно система энергию свою никогда повышать не станет, она всегда стремится ее уменьшить. Именно поэтому предоставленная сама себе капля воды принимает форму шара: ведь сфера — это наименьшая площадь поверхности для тела данного объема.
Несколько искаженный шар представляет собою капля ртути, помещенная на стекло. А вот если вы капнете на чистое стекло воду, никаких капель не получится, вода равномерно растечется по стеклу. Почему такая разница? Дело в том, что атомы ртути гораздо сильнее притягиваются друг к другу, чем к молекулам, составляющим стекло. Молекулы же воды более склонны прилипать к частицам стекла. Взаимодействие воды и ртути со стеклом — это два крайних случая: здесь говорят о полном смачивании и полном несмачивании стекла.
Теперь нетрудно объяснить загадку, с которой начиналась статья: почему прилипает бумажный лист к пальцу, смоченному водой? В условиях полного смачивания капля воды, находящейся между пальцем и бумагой, имеет форму, изображенную на рисунке. Чтобы отдалить палец от бумаги, необходима известная сила, необходима затрата энергии, поскольку при этом боковая поверхность капли увеличивается.

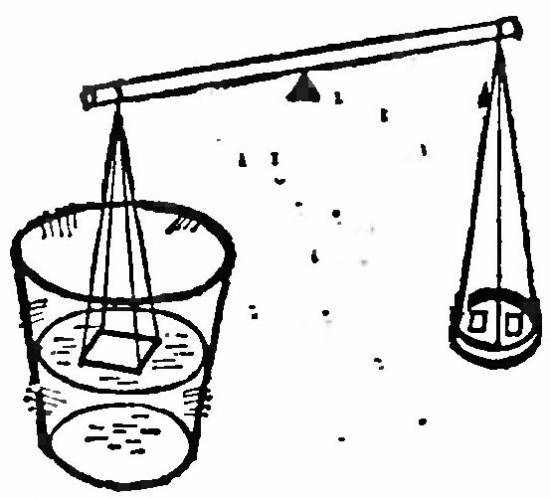
От этого объяснения недалеко до описания простенького опыта, позволяющего оценить поверхностное натяжение различных жидкостей. Соорудите весы из стеклянной, металлической или деревянной палочки и нескольких ниток. Одну чашку можно сделать из алюминиевой фольги, а вместо другой используйте квадрат, согнутый из тонкой медной проволоки. Приведите коромысло весов в горизонтальное положение, положив на чашку какой-нибудь груз (скажем, немного пластилина). Теперь подставьте под квадрат из проволоки стакан с водой так, чтобы квадрат «прилип» к поверхности. Накладывая постепенно на чашку весов «гирьки» (например, вырезанные из фольги кусочки одинаковой площади) и отметив момент, когда квадрат оторвется от поверхности, мы в каких-то условных единицах измерим поверхностное натяжение.
Па практике коэффициент поверхностного натяжения обычно измеряют в эргах на квадратный сантиметр. Для воды при 20° С он составляет 73 эрг/см2. Замените воду на спирт, и вы увидите, что поверхностное натяжение у этой жидкости гораздо меньше (22 эрг/см2). У глицерина оно почти такое же, как у воды (62 эрг/см2).
А теперь растворите в стакане воды небольшой кусочек мыла и определите поверхностное натяжение такого раствора. Вы увидите, что поверхностное натяжение воды после растворения мыла резко снизилось.
Молекулы веществ, из которых состоит мыло, несут на одном своем конце карбоксильную группу СООН, в которой атом водорода заменен на ион щелочного металла: СООNa. Эта часть молекулы мыла охотно притягивается к молекулам воды, завязывая с ними водородные связи. Кроме этого, у мыльной молекулы есть длиннющий хвост, который состоит из углеродных атомов, окруженных атомами водорода, скажем, СН3 (СН2)16, если мыло изготовлено на основе стеариновой кислоты. Звенья такого хвоста не проявляют никакого расположения к молекулам воды: все связи, которые могут завязать между собою атомы углерода и водорода, здесь завязаны, на образование побочных связей нет ни грана электронной плотности.
Когда молекула мыла попадает в воду, ее карбоксильная часть окружает себя молекулами воды, чего не скажешь про хвост; в результате молекула оказывается на поверхности, ее хвост распластан на самой границе вода — воздух, а карбоксильная «головка» утоплена в объем воды.
Исследуем некоторые физико-химические свойства поверхностного слоя мыла. Для этой цели нам послужит весьма остроумный прибор, называемый весами Лэнгмюра. Его устройство ясно из рисунка. В прямоугольной ванне с одного края имеется ограничитель, позволяющий изменять площадь ванны. На другом конце ванны размещается подвижный поршень, связанный с очень тонкой пружиной и стрелкой, которая отражает давление, оказываемое на поршень.
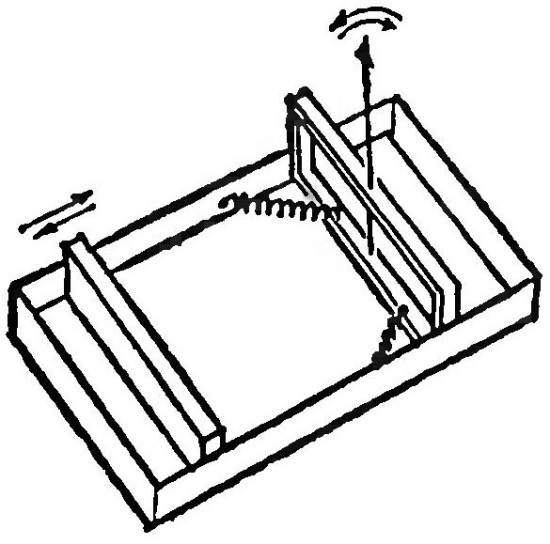
Капните мылом на поверхность воды. Молекулы мыла будут стремиться «растечься» по поверхности, то есть увеличить площадь своего обитания, но поршень мешает им сделать это. Поэтому на поршень будет оказываться давление, которое можно измерить по отклонению стрелки (к стрелке приспособьте шкалу с условными делениями).
Будем теперь уменьшать площадь ванны, передвигая ограничитель. Если на графике откладывать по оси абсцисс площадь S, занимаемую молекулами мыла, а по оси ординат давление Р, оказываемое на поршень, то на каком-то определенном участке АВ давление Р будет расти по мере уменьшения площади S. Произведение давления на площадь оказывается при этом постоянным. Это напоминает поведение газа при постоянной температуре, описываемое законом Бойля—Мариотта. Можно сказать, что мы имеем дело как бы с двумерным газом. Это потому, что молекулы мыла находятся (так же как и молекулы газа) на значительном расстоянии друг от друга, как показано на рисунке. Черные точки — это группы COONa, зигзагами обозначены углеводородные хвосты.
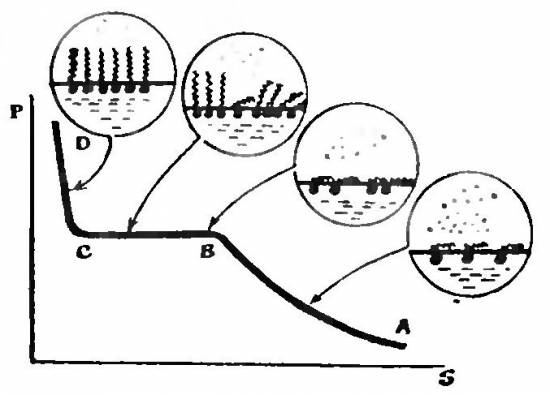
Продолжаем уменьшать площадь S. В точке В мы приходим к такой ситуации, когда вся поверхность занята распластанными молекулами мыла. Дальше при сжатии молекулам становится так тесно, что некоторые из них начинают поднимать хвосты над поверхностью воды, число же распластанных молекул на единицу площади при этом будет оставаться прежним. А это значит, что давление на поршень меняться не будет (участок ВС).
Наконец, мы приходим в точку С, когда все молекулы плотно прижаты друг к другу и у всех хвосты торчат над поверхностью. Теперь слой мыла будет вести себя как несжимаемая двумерная жидкость: небольшое уменьшение площади станет приводить к резкому повышению давления.
Зная количество нанесенного на поверхность мыла и площадь ванны в моменты В и С, нетрудно рассчитать длину одной распластанной молекулы, вычислить диаметр хвоста молекулы. (Напомним, что в грамм-молекуле вещества содержится 6•1023 молекул; молекулярный вес мыла, если оно создано на основе стеариновой кислоты, равен 306.)
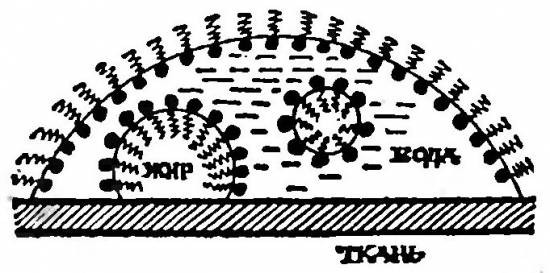
Почему же мыло обладает моющими свойствами? Здесь много причин. Мы уже определили, что мыло резко (более чем в два раза) понижает поверхностное натяжение воды. А это значит, что мыльная вода может проникать в самые мельчайшие поры на ткани, смачивая все самые удаленные уголки, куда попали загрязнения. На границе воды и капельки жирового загрязнения молекулы мыла расположатся так, что карбоксильные группы окажутся в воде, а углеводородные хвосты — в жире (они ведь и сами образованы жироподобным веществом, а согласно старинному правилу химии, подобное растворяется в подобном). Таким образом молекулы мыла разорвут жир на мелкие капли и утянут их в воду. Образуется эмульсия, которую нетрудно удалить — стоит только хорошенько потереть ткань в мыльной воде, а потом прополоскать.
Мыло нетрудно получить из жиров, которые представляют собой сложные эфиры глицерина и высших жирных кислот, например, стеариновой. Если подействовать на жир щелочью, образуется соль стеариновой кислоты — иными словами, мыло. В стакане смешайте половину чайной ложки твердого жира с несколькими ложками раствора едкого натра в спирте. Нагревайте смесь несколько минут в кастрюле с горячей водой. Когда раствор станет однородным, охладите его и добавьте к нему насыщенный водный раствор поваренной соли. Через несколько минут на поверхности выделится слой мыла. |  Поддержать проект
Поддержать проект Поддержать проект
Поддержать проект