 С каждым годом хозяйки все чаще пользуются при стирке специальными порошками. Их преимущество по сравнению с мылом неоспоримо. С каждым годом хозяйки все чаще пользуются при стирке специальными порошками. Их преимущество по сравнению с мылом неоспоримо.
Откуда у моющих средств такие качества? Каким образом удалось химикам их получить? От чего зависят их свойства?
Молекулы моющих средств всегда состоят из двух частей: гидрофильной и гидрофобной.
Гидрофильная часть — это кислота. Соли кислот обычно растворяются в воде, примерно как столовая соль, и увлекают за собой в раствор всю молекулу. Другой конец молекулы, гидрофобный, напротив, отличается сильным сродством к жирным веществам и органическим растворителям. Эта двойственность достигается путем присоединения к молекуле органического радикала — длинной цепи атомов углерода или ядра бензола. Молекулы моющих средств склонны к тому же скапливаться на поверхности раствора, образуя пленку из молекул, гидрофобные окончания которых «нацелены» в воздух и с водой не соприкасаются. При столкновении с жирным пятном «головы» молекул моющего вещества погружаются в жир, а «хвосты» плавают в воде. Таким образом и происходит соединение воды и жирных тел.
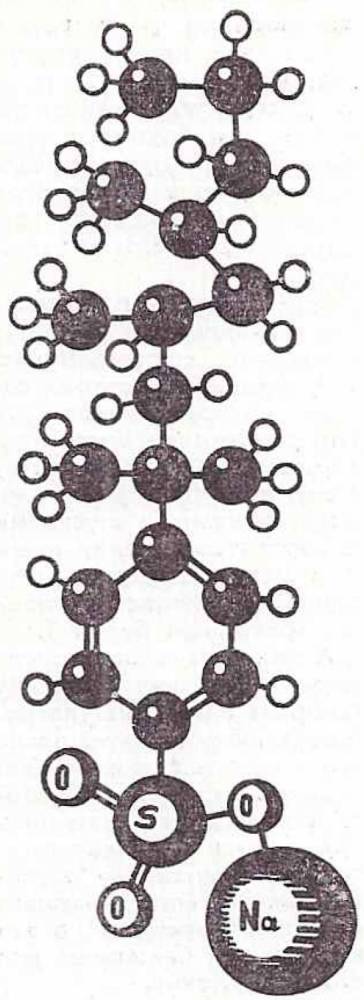
На этой схеме — структура молекулы моющего средства. Нижняя часть этой структуры представляет собой гидрофильную «головку». Ее свойствами объясняется растворимость моющего сродства в воде.
Верхняя часть структуры — гидрофобный (водоотталкивающие;) «хвост» молекулы. Им определяется сродство; между моющим средством и жирными веществами, а также органическими растворителями.
Этими противоположными свойствами и объясняется способность моющего средства удалять жировые пятна.
Склонность молекул моющих средств собираться на свободной поверхности воды приводит к изменению свойств этой поверхности. Уменьшается поверхностное натяжение, вода лучше смачивает твердые тела, а это очень важно при стирке.
Изменение поверхностного натяжения способствует также образованию пены. Тончайшие слои воды с двух сторон одеваются пленками моющего средства, молекулы которого скапливаются на поверхности пузырька. Действие пены во время стирки является механическим: пузырьки, проходя через волокна ткани, отделяют и уносят частички внедрившейся туда грязи.
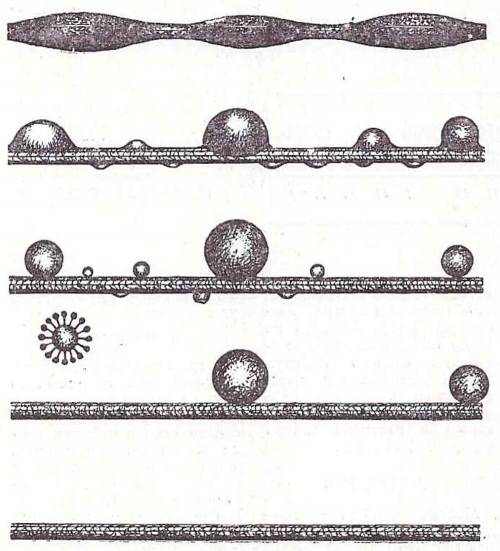
Как действует моющее средство?
Первая (верхняя) ступень схемы — волокно, покрытое жировой оболочкой. Следующие дне ступени — молекулы моющего средства обволакивают жировой слой, абсорбируют его. Следующий этап — жир собирается в отдельные шарики, а затем, наконец, полностью удаляется с поверхности волокна. Внизу — чистая ткань.
Как видите, возможности моющих средств разнообразны: они помогают смачивать предмет, снимать жиры, эмулыировать их, растворять и образовывать пену.
В зависимости от назначения моющего средства предпочтение отдается тому или иному его свойству. Так, стиральные порошки должны состоять из активных, концентрированных моющих средств, включать в себя отбеливающие и сильные щелочные компоненты. Наоборот, шампуни для мытья волос должны содержать главным образом высококачественные пенящиеся вещества.
В основе 75% стиральных порошков, продающихся во всем мире, лежит одно соединение — алкил-бензол-сульфонат натрия.
Алкил-бензол-сульфонаты — производные бензола, одного из основных исходных веществ химической индустрии. Молекула бензола построена в виде шестиугольного кольца. Чтобы получить моющее средство, к этому кольцу нужно присоединить цепь атомов углерода, с одной стороны, и группу сульфоната натрия — с другой. Это типичная операция в промышленности органического синтеза: к основной молекуле последовательными этапами прибавляют определенные составные части, чтобы получить вещество с заранее заданными свойствами.
В названии «алкил-бензол-сульфонат» слова «бензол» и «сульфонат» обозначают две части синтезированной молекулы. Слово «алкип» обозначает третью часть — цепь атомов углерода, которую «прививают» к молекуле бензола. Эта цепь может быть более или менее длинной, содержать большее или меньшее количество атомов углерода, соединенных друг с другом. Существует целая семья алкил-бензолов, которые различаются между собой длиной этой цепи.
Это не значит, что цепь можно выбрать наугад: от ее длины зависит качество получаемого продукта. Если она коротка и насчитывает не более 3—10 атомов углерода, полученное соединение будет хорошо растворяться в воде, но его моющие качества будут посредственными. Цепь, состоящая из 14 атомов и больше, даст моющее средство, которое хорошо пенится и переводит жиры в раствор, но само при этом плохо растворяется. Компромиссное решение — 12 атомов углерода. Наиболее распространенные моющие средства — додецил-бензол-сульфонаты. Их молекула содержит бензольное шестиугольное кольцо, присоединенное к цепи из 12 атомов углерода и к группе сульфоната натрия.
Создать эффективное моющее средство — это далеко не все. От него еще надо и избавиться. И вот эта задача представляет собой настоящую головоломку.
Обычное мыло ведет себя очень скромно. Когда его после употребления выбрасывают в виде мыльной воды, оно исчезает, Оно не просто растворяется в реках и подземных водах, оно преобразуется совершенно. Синтетические моющие средства — увы! — не так хорошо «воспитаны».
После употребления они остаются в воде невредимыми. Если бы их можно было каким-то образом из соды извлечь, они вполне годились бы для использования во второй и в третий раз: их свойства не изменяются. А так как их никто не трогает, они о водоемах упрямо продолжают делать то, чему их научили: они пенятся.
От чего зависит эта существенная разница в поведении мыла и его синтетических соперников? И прежде всего, что заставляет мыло исчезнуть?
Микрофлора почвы и рек питается тем, что находится в воде. И если бактериям попадается мыло, они включают его в свое меню. Они разлагают молекулу мыла на более простые элементы и усваивают их — так, как мы усваиваем, например, белки из мяса. Специалисты говорят, что мыло является «биоусвояемым»: его молекула может быть разложена и ассимилирована микроорганизмами.
Большая часть синтетических моющих средств не биоусвояема. Бактерии не хотят их поглощать, отказываются «демонтировать» их молекулу, чтобы сделать из нее безвредные составные части.
Как только ученые заметили, что этот чудесный подарок химии хозяйкам совершенно не пришелся по вкусу бактериям, они стали искать причину этой несовместимости. Причина, конечно, оказалась в молекуле моющего средства.
Установлено, что ни бензольное ядро, ни группа сульфоната натрия, присутствующие в молекуле моющих средств, не повинны в том, что бактерии отказываются усваивать молекулу. Остается только один возможный виновник — это группа из 12 атомов углерода.
Эта группа получается при соединении четырех маленьких составных частей, каждая из которых состоит из трех атомов. Эти четыре цепочки могут присоединяться друг к другу различным образом. Они могут сцепляться «гуськом» и образовывать одну длинную цепь. Но они могут также соединиться в форме креста или буквы Т.
А это, оказывается, очень существенно для бактерий, которым предстоит употребить в пищу продукт после его использования. Они принимаются за свою работу в том случае, если цепь прямая, но они бессильны перед «ветвистыми» молекулами. Ветвистость мешает окислению продукта, а это необходимо бактериям для его разрушения.
Каким же образом можно получить «усвояемые» стиральные порошки?
Если продолжать использовать обычный основной продукт — алкил-бензол-сульфонат, то молекулу с разветвленной группой углерода следует заменить ее биоусвояемым вариантом с прямой цепью. Направить синтез так, чтобы получать только прямые молекулы, не представляется возможным. Нужно отбирать необходимые молекулы из смеси. Казалось бы, это невозможно, но тем не менее такой отбор уже делается.
Существуют современные методы сортировки с помощью так называемого «молекулярного сита». Молекулы, которые нужно рассортировать, пропускаются через отверстия такие крохотные, что ветвистые молекулы сквозь них не проходят.
Можно вообще отказаться от средств, полученных на базе алкил-бензол-сульфоната, и заменить их другими продуктами, которые по качеству останутся такими же, но благодаря совершенно другой структуре будут биоусвояемыми. Вместо того, чтобы создавать продукты, так непохожие на повседневное меню бактерий, как эти злосчастные молекулы, специалисты занимаются сейчас созданием привычных для микроорганизмов длинных цепей, аналогичных цепям жирных кислот. В их формуле совсем нет бензола, но сульфонатная группа, без которой продукт не будет моющим средством, должна присутствовать обязательно.
Группа немецких ученых из Франкфурта создала моющее средство, биоусвояемое на 100% и по качеству не уступающее самым лучшим продуктам. Исходными для него были жирные кислоты, спирт и различные сахара.
Каким бы путем ни шли ученые, они преследуют одну цель: новые моющие средства должны представлять вполне подходящую пищу для бактерий и вернуть рекам покой.
Сокращенный перевод с французского |  Поддержать проект
Поддержать проект Поддержать проект
Поддержать проект